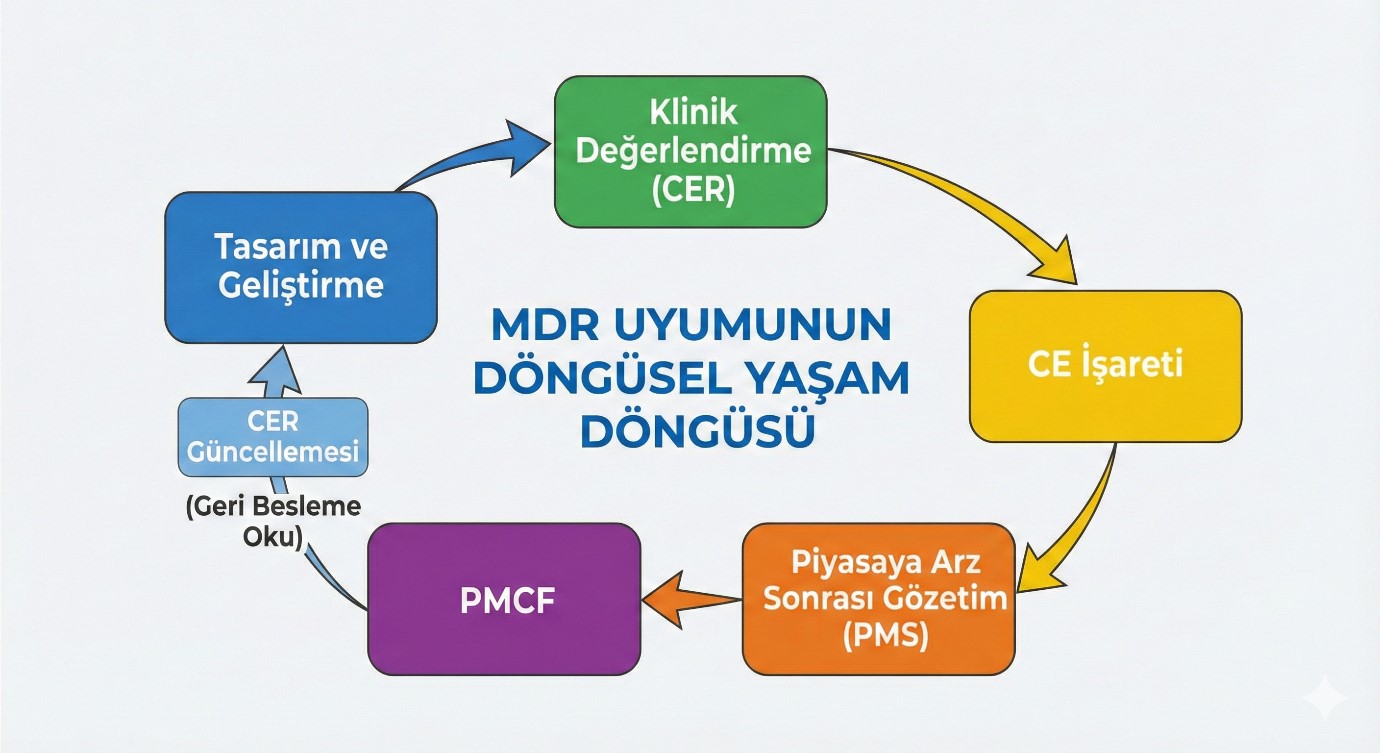
MDR’ın Yaşam Döngüsü Yaklaşımı: PMCF’nin Kritik Rolü
Tıbbi Cihaz Yönetmeliği (MDR), bir cihazın CE işaretini almasıyla regülatif sürecin sona ermediği, aksine yeni bir aşamaya, yani yaşam döngüsü yönetimine geçildiği ilkesine dayanır. Bu yaşam döngüsünün en kritik bileşenlerinden biri, Piyasaya Arz Sonrası Klinik Takip (PMCF – Post-Market Clinical Follow-up)’tir.
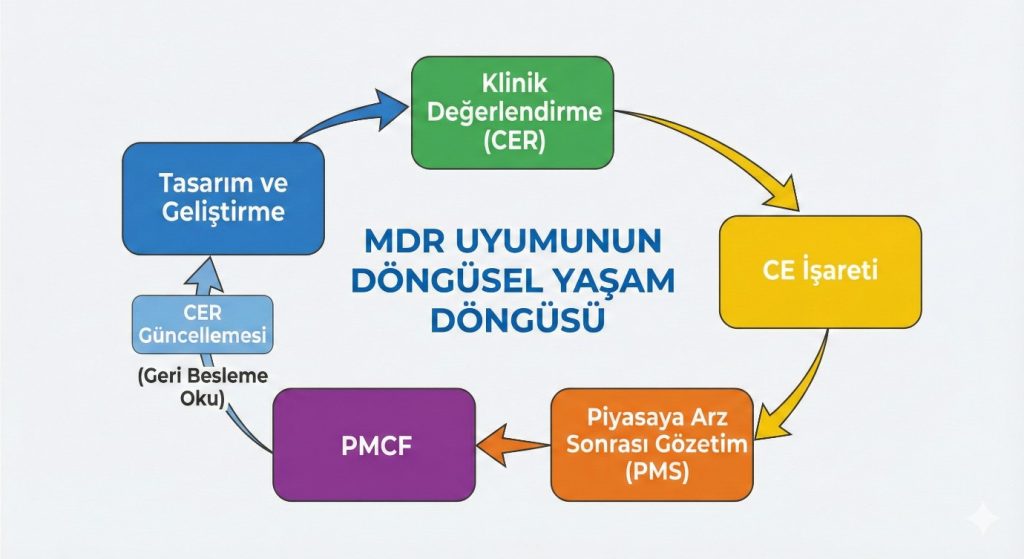
Şekil 1: MDR Yaşam Döngüsü (Cycle Diagram)
PMCF, cihazın piyasaya sürüldükten sonra, amaçlanan kullanım koşullarında güvenliğini ve performansını sürekli olarak izlemek ve Klinik Değerlendirme Raporu’nu (CER) güncel tutmak için proaktif olarak klinik veri toplama sürecidir.
PMCF’nin Amacı: Gerçek Dünya Verileriyle Kanıt
PMCF’nin temel amacı, cihazın piyasaya sürülmeden önce toplanan klinik verilerle (Bölüm 5 ve 6) ele alınamayan konuları ele almaktır:
- Uzun Vadeli Güvenlik ve Performans: Cihazın uzun süreli kullanımının potansiyel etkilerini ve nadir görülen yan etkileri tespit etmek.
- Kalan Risklerin Doğrulanması: Risk Yönetimi sürecinde belirlenen kalan risklerin gerçek hayatta kabul edilebilirliğini doğrulamak.
- Yeni Risklerin Tespiti: Piyasada ortaya çıkabilecek yeni riskleri veya yanlış kullanımları erken aşamada belirlemek.
- CER’in Güncellenmesi: Toplanan verileri kullanarak CER’i sürekli olarak güncel tutmak ve cihazın GSPR’lere (Genel Güvenlik ve Performans Gereklilikleri) uygunluğunu sürdürmek.
PMCF Süreci: Proaktif ve Planlı Yaklaşım
PMCF, rastgele bir veri toplama süreci değil, sistematik ve planlı bir yaklaşımdır.
- PMCF Planı (PMCF Plan)
Her üretici, cihazının risk sınıfına ve özelliklerine uygun bir PMCF Planı hazırlamak zorundadır. Bu plan, hangi klinik verilerin, hangi yöntemlerle (anketler, hasta kayıtları, yeni PMCF çalışmaları vb.) ve hangi sıklıkta toplanacağını detaylandırır.
- Veri Toplama ve Analiz
Plan doğrultusunda veriler toplanır. Bu veriler, şikayet kayıtları, literatür taraması, kullanıcı anketleri veya özel olarak tasarlanmış PMCF çalışmaları (klinik araştırmalar) olabilir. Toplanan veriler, cihazın fayda-risk oranını etkileyip etkilemediğini belirlemek için analiz edilir.
- PMCF Değerlendirme Raporu (PMCF Evaluation Report)
Analiz sonuçları, belirlenen periyotlarda (genellikle yılda bir) PMCF Değerlendirme Raporu’nda özetlenir. Bu rapor, CER’in güncellenmesi için temel teşkil eder ve Teknik Dokümantasyonun bir parçasıdır.
Sürekli Uyum ve Piyasaya Arz Sonrası Gözetim (PMS)
PMCF, daha geniş bir süreç olan Piyasaya Arz Sonrası Gözetim (PMS – Post-Market Surveillance) sisteminin bir parçasıdır. PMS, üreticinin cihazın tüm yaşam döngüsü boyunca proaktif ve reaktif olarak güvenlik verilerini topladığı, kaydettiği ve analiz ettiği tüm faaliyetleri kapsar.
Süreç | Kapsam | Odak Noktası |
PMS (Piyasaya Arz Sonrası Gözetim) | Reaktif ve Proaktif tüm faaliyetler (Şikayet yönetimi, güvenlik raporlaması, trend analizi). | Cihazın piyasada güvenliğinin genel takibi. |
PMCF (Piyasaya Arz Sonrası Klinik Takip) | PMS’in proaktif klinik veri toplama bileşeni. | Cihazın klinik performansının ve CER’in doğrulanması/güncellenmesi. |
MedicalPoint Klinik Araştırmalar Merkezi’nin (MPH-KAM) PMCF ve Sürekli Uyum Desteği
MDR, üreticilerden sadece bir kerelik CE onayı değil, sürekli bir regülatif uyum taahhüdü bekler. MPH-KAM olarak, bu döngüsel süreci yönetmenize yardımcı oluyoruz:
- PMCF Planı Hazırlığı: Cihazınızın risk profiline uygun, maliyet-etkin ve MDR uyumlu PMCF planlarının oluşturulmasına medikal destek
- PMCF Çalışmalarının Yürütülmesi: Gerekli görülen durumlarda, PMCF klinik araştırmalarının (örneğin, uzun dönem takip çalışmaları) uluslararası GCP standartlarında yürütülmesi.
- CER Güncelleme Desteği: PMCF verileri ışığında CER’in düzenli olarak güncellenmesi ve Teknik Dokümantasyonun denetime hazır tutulmasına yüksek kalitede veri desteği
Bu sürekli gözetim ve veri toplama döngüsü, cihazınızın pazar güvenilirliğini artırır ve Onaylanmış Kuruluş denetimlerinde başarılı olmanızı sağlar.
Referanslar
[1] Regulation (EU) 2017/745 of the European Parliament and of the Council of 5 April 2017 on medical devices, Article 83.
[2] MDCG 2020-7 Guidance on PMCF Plan and Report. European Commission.
[3 The Role of PMCF in the Medical Device Lifecycle. NAMSA.