Tıbbi Cihaz Klinik Araştırmalarının Fazları ve Yönetimi
İlaç çalışmalarının aksine, tıbbi cihaz klinik araştırmaları (Clinical Investigations – CI) genellikle fazlara ayrılmaz. Ancak, MDR’ın gerektirdiği klinik kanıtın toplanması süreci, cihazın gelişim aşamasına göre mantıksal olarak aşamalara ayrılabilir. Bu aşamalar, cihazın güvenliğini ve performansını aşamalı olarak kanıtlamayı hedefler.
Aşama | Amaç | Odak Noktası |
Erken Feasibility (Fizibilite) | Cihazın temel tasarımının ve çalışma prensibinin insan üzerinde güvenli olup olmadığını doğrulamak. | Az sayıda hasta, kısa süreli takip, temel güvenlik verileri. |
Pivotal Çalışma | Cihazın amaçlanan klinik faydayı sağladığını ve güvenli olduğunu istatistiksel olarak kanıtlamak. | Yeterli sayıda hasta, uzun süreli takip, birincil ve ikincil etkinlik/güvenlik sonlanım noktaları. |
Piyasaya Arz Sonrası (PMCF) | Cihazın uzun vadeli güvenliğini ve performansını gerçek dünya koşullarında izlemek. | Çok sayıda hasta, uzun süren takip, nadir görülen yan etkilerin tespiti. |
Klinik Araştırma Yönetiminde Başarının Anahtarı
Başarılı bir klinik araştırma, sadece bilimsel olarak sağlam olmakla kalmaz, aynı zamanda regülatif açıdan da kusursuz olmalıdır. Yönetim sürecinde kritik başarı faktörleri şunlardır:
- Stratejik Planlama (CIP): Araştırmanın, CER’in ihtiyaç duyduğu spesifik GSPR’leri (Genel Güvenlik ve Performans Gereklilikleri) hedef alacak şekilde tasarlanması.
- Regülatif Hız: Etik Kurul ve Yetkili Otorite (TİTCK) onay süreçlerinin hatasız yönetilmesi.
- Veri Kalitesi: ISO 14155 (GCP) standartlarına tam uyum ve güvenilir veri toplama sistemlerinin kullanılması.
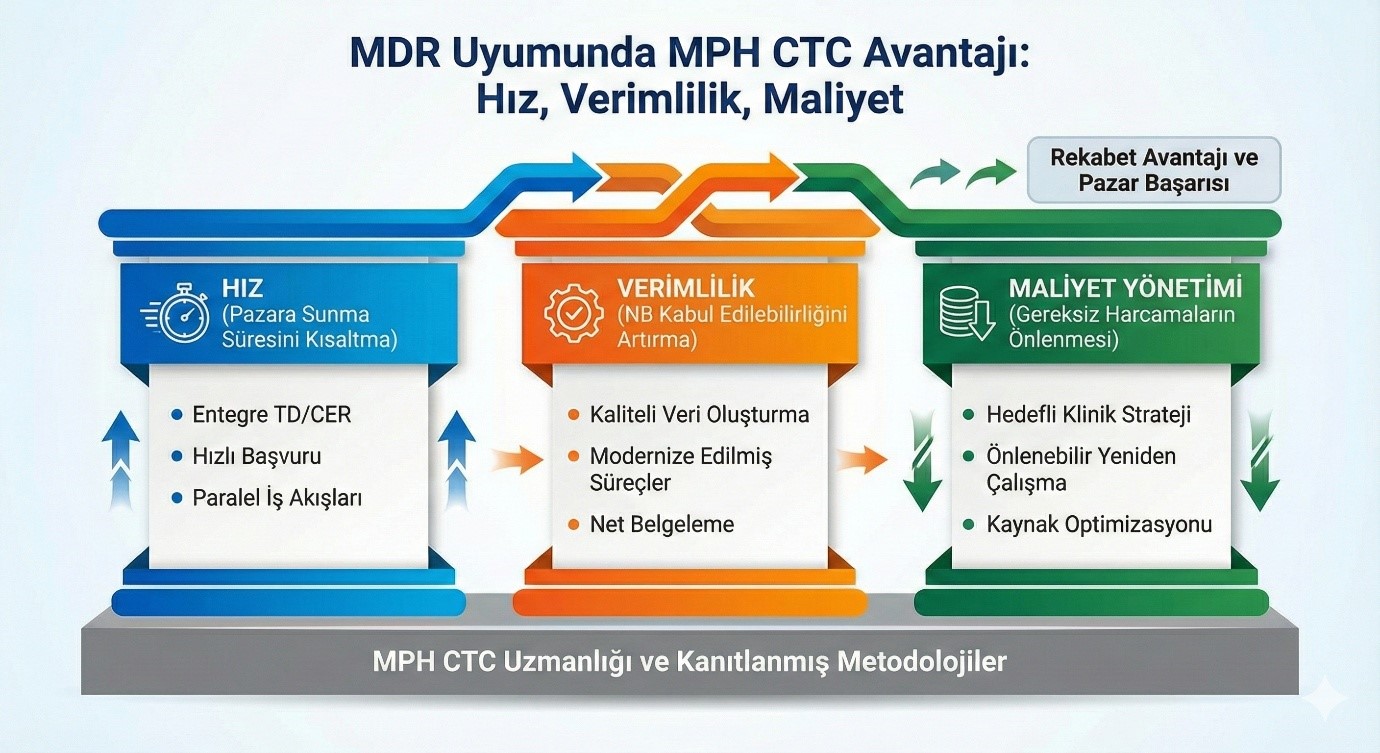
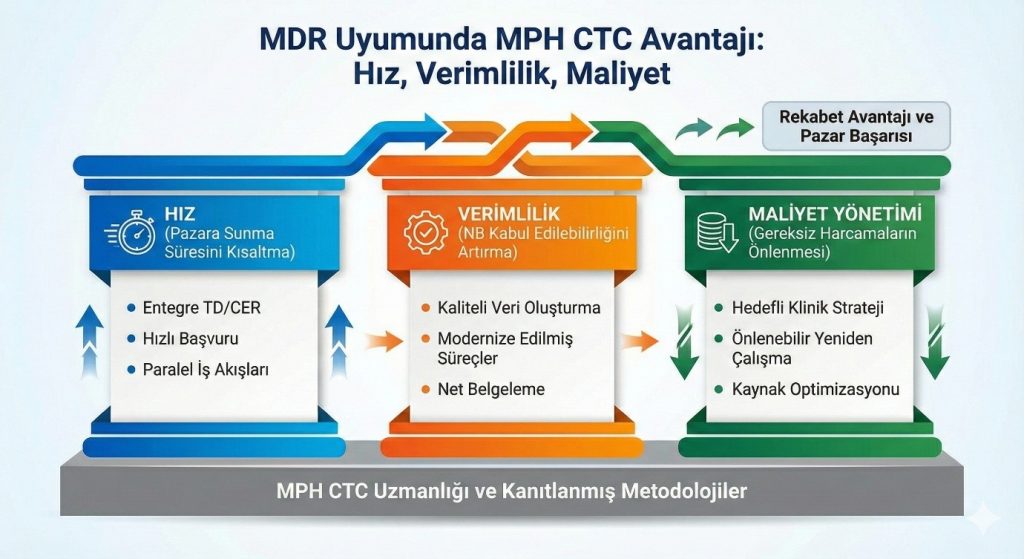
MDR Süreçlerinde Hız, Etkinlik ve Maliyet Yönetimi
MDR uyum süreci karmaşık, zaman alıcı ve maliyetlidir. MPH-KAM olarak, bu zorlu süreçte üreticilere rekabet avantajı sağlayan üç temel sütun üzerine odaklanıyoruz: Hız, Etkinlik ve Maliyet Yönetimi.
- Hız: Pazara Erişim Süresini Kısaltma
Regülatif süreçlerdeki gecikmeler, pazara giriş fırsatlarının kaçırılması anlamına gelir. Hız avantajımızı sağlayan temel stratejilerimiz:
- Hızlı Başvuru Yönetimi: Etik Kurul başvurularını, TİTCK regülatif gerekliliklere tam hakimiyetimiz sayesinde ilk seferde onay alacak şekilde hazırlığı hususunda tıbbi destek ( Protokol hazırlığı, örneklem büyüklüğü seçimi)
- Geniş Gönüllü Havuzu: Hasta alımını (recruitment) hızlı tutmak için çeşitli branşlarda geniş hasta populasyonu
- Etkinlik: Veri Kalitesini ve Kabul Edilebilirliği Artırma
- GCP Uzmanlığı: Tüm tıbbi cihaz klinik araştırmalarını, uluslararası kabul görmüş ISO 14155 (GCP) standartlarına uygun olarak yürütmek.
- CER-Odaklı Tasarım: Araştırmaları, CER’in ihtiyaç duyduğu spesifik klinik sonlanım noktalarını kanıtlayacak şekilde tasarlamak.
- Uzman Kadro: Regülatif uzmanlar, biyoistatistikçiler ve klinik araştırma koordinatörlerinden oluşan deneyimli ekibimizle sürecin her aşamasını yönetmek.
- Maliyet Yönetimi: Gereksiz Harcamaları Önleme
- Doğru Sınıflandırma ve Strateji: En başta doğru risk sınıflandırması yaparak, gereksiz NB denetimlerinden veya fazla klinik veri toplama yükünden kaçınmak.
- Tek Merkezli Çözüm: Klinik araştırma, regülatif danışmanlık ve tıbbi yazım hizmetlerini tek bir çatı altında sunarak koordinasyon maliyetlerini düşürmek.
Referanslar
[1] Regulation (EU) 2017/745 of the European Parliament and of the Council of 5 April 2017 on medical devices, Annex XV.
[2] ISO 14155:2020 Clinical investigation of medical devices for human subjects — Good clinical practice.
[3] MDCG 2020-5 Guidance on clinical evaluation – equivalence.European Commission.