Özet: Klinik araştırmalar dünyası 2026 yılı itibarıyla veri bilimi, yapay zeka ve sofistike regülatif stratejilerin iç içe geçtiği çok boyutlu bir teknoloji ekosistemine dönüşmüştür(1). Bu makale; sentetik kontrol kolları, yapay zeka tabanlı protokol otomasyonu ve 2026 yılındaki küresel regülatif güncellemeleri akademik bir perspektifle incelemektedir (2).
- Giriş
Klinik araştırmalar, tıbbi bilginin üretilmesi ve yeni tedavilerin güvenilirliğinin test edilmesi süreçlerinde tarihsel bir dönüm noktasından geçmektedir (3). Geleneksel randomize kontrollü çalışmaların (RCT) altın standart olma özelliği korunmakla birlikte; maliyet kısıtları, etik endişeler ve hasta katılımı zorlukları sektörü dijital ikizler ve sentetik kontrol kolları gibi yenilikçi modellere yöneltmiştir (4).
- Metodolojik Yenilikler: Sentetik Kontrol Kolları (SCA)
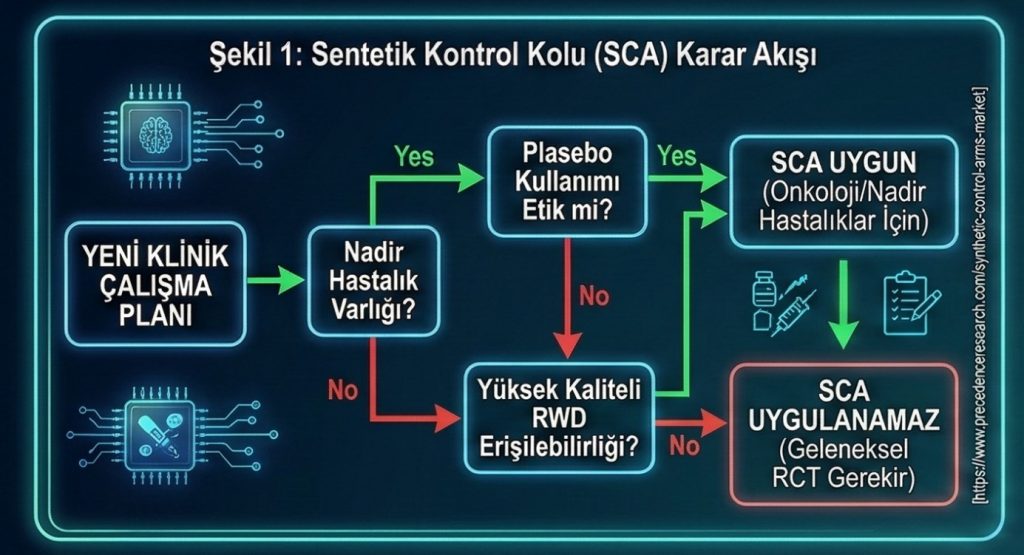
Sentetik Kontrol Kolları (SCA), gerçek dünya verilerini (RWD) veya geçmiş klinik araştırma verilerini kullanarak, bir çalışmaya yeni hastalar dahil etmeden sanal bir karşılaştırıcı grup oluşturulması sürecidir (4). 2026 yılı itibarıyla bu yöntemin klinik başarıları ve pazar verileri şu şekildedir:
- Etik Avantaj: Özellikle onkoloji ve nadir hastalıklarda, hastaların plasebo grubuna düşme riskini ortadan kaldırarak her katılımcının aktif tedaviye erişimini sağlar (5).
- Veri Paylaşımı ve Başarı: 2025 yılında sunulan geniş kapsamlı onkoloji çalışmaları, yapay zeka ile oluşturulan sentetik veri setlerinin sağkalım analizlerinde orijinal verilerle tam uyum gösterdiğini kanıtlamıştır (6).
- Pazar Dağılımı: 2026 projeksiyonlarına göre, SCA teknolojilerinde gerçek dünya verileri (RWD) %53,50 ile liderliği sürdürürken, yapay zeka tabanlı analiz platformları %37.50’lik bir pazar payına sahiptir (4).
- Yapay Zekâ ve Protokol Otomasyonu
Yapay zeka, 2026 yılında klinik operasyonların temel taşı haline gelmiştir (7). Özellikle protokol tasarımı ve veri yönetimi alanlarındaki etkisi somuttur:
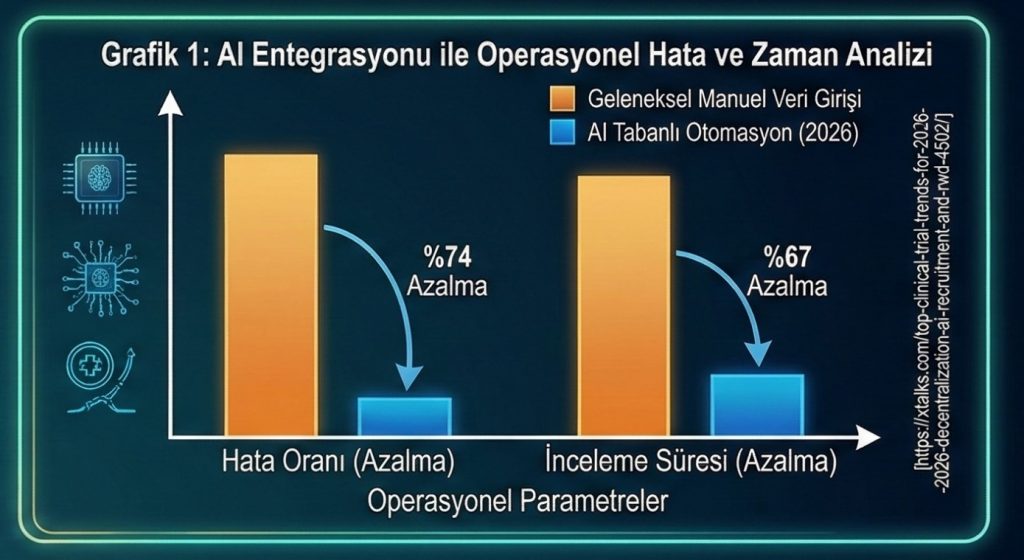
- Verimlilik Artışı: Yapay zekâ destekli elektronik klinik sonuç değerlendirme (eCOA) iş akışları, veri hatalarını %74 oranında azaltırken, inceleme döngülerini %67 oranında kısaltmıştır (2).
- Dijitalleşme: PDF formatındaki protokollerin otomatik olarak elektronik veri tabanlarına (EDC) dönüştürülmesi ve yapay zekanın geçmiş verileri kullanarak yeni deneme protokolleri yazması (digitalization), kurulum sürelerini minimize etmektedir (7).
- Regülatif Dönüşüm: FDA, EMA ve TİTCK Güncellemeleri
Teknolojik ilerlemeler, regülatif otoritelerin “kanıt optimizasyonu” odaklı yeni politikalar benimsemesini (8):
- FDA (19 Şubat 2026): FDA, belirli şartlar altında tek bir pivot çalışmanın onay için yeterli olabileceğini resmi olarak onaylamıştır (8). Bu durum, biyobelirteç uyumu ve gerçek dünya kanıtlarıyla desteklenen “toplam kanıt ekosistemi” yaklaşımını zorunlu kılmaktadır (8). Ayrıca ultra nadir hastalıklar için “Plausible Mechanism” çerçevesi yayınlanmıştır (9).
- EMA (15 Ocak 2026): Avrupa İlaç Ajansı, pazarlama sonrası süreçlerin dijitalleşmesini ve daha verimli hale getirilmesini sağlayan yeni Varyasyon Kılavuzunu yürürlüğe koymuştur (10). Mart 2026 itibarıyla yürürlüğe giren ICH M14 kılavuzu ise gözlemsel verilerin güvenlik değerlendirmelerinde kullanımı için uluslararası standartlar getirmiştir (11).
- TİTCK (14 Kasım 2025): Türkiye’de klinik araştırma başvurularında uluslararası kabul görmüş İyi Laboratuvar Uygulamaları (GLP) sertifikası sunulması zorunlu hale getirilmiştir (12).
- Desantralize Klinik Denemeler (DCT)
Hibrit ve merkezi olmayan modeller, giyilebilir teknolojiler sayesinde 2026’da standart bir uygulama haline gelmiştir (2). Giyilebilir cihazlar, uyku ve hareket gibi 200’den fazla parametreyi sürekli izleyerek, hastaların merkeze gitme yükünü azaltmakta ve veri kalitesini artırmaktadır (2).
- Sonuç
Klinik araştırmalar, yapay zekanın analitik gücüyle daha hızlı, etik ve hasta merkezli bir yapıya evrilmektedir (13). 2030 yılına kadar 190 milyar dolara ulaşması beklenen yapay zekâ pazarı, bu dönüşümün kalıcı ve stratejik olduğunu göstermektedir (1).
- Gündüz Y. Haberler. hospitalmanager [İnternet]. [a.yer 04 Mart 2026]. Erişim adresi: https://www.hospitalmanager.com.tr/haberler/
- MBiotech SS. Top Clinical Trial Trends for 2026: Decentralization, AI Recruitment and RWD. Xtalks [Internet]. 24 Kasım 2025 [a.yer 04 Mart 2026]. Erişim adresi: https://xtalks.com/top-clinical-trial-trends-for-2026-decentralization-ai-recruitment-and-rwd-4502/
- Clinical Research in 2026:What’s Changing and Why It Matters [Internet]. 22 Ocak 2026 [a.yer 04 Mart 2026]. Erişim adresi: https://cromospharma.com/clinical-research-in-2026-what-changed-and-why-it-matters/
- Synthetic Control Arms Market Size, Report by 2034 [Internet]. [a.yer 04 Mart 2026]. Erişim adresi: https://www.precedenceresearch.com/synthetic-control-arms-market
- nashvillebios. Synthetic Control Arms in Clinical Trials. Nashville Biosciences [Internet]. 18 Aralık 2024 [a.yer 04 Mart 2026]. Erişim adresi: https://nashbio.com/blog/clinical-trials/synthetic-control-arms-in-clinical-trials/
- How AI is expediting clinical research: the use of synthetic real-world data [Internet]. [a.yer 04 Mart 2026]. Erişim adresi: https://dailyreporter.esmo.org/esmo-ai-digital-oncology-congress-2025/editorial/how-ai-is-expediting-clinical-research-the-use-of-synthetic-real-world-data
- Trends for 2026: Targeted AI, continuous trials, and navigating uncertainty [İnternet]. [a.yer 04 Mart 2026]. Erişim adresi: https://www.merative.com/blog/clinical-trial-trends-2026
- FDA’s Shift to One Pivotal Trial for Drug Approval: Strategic Implications for Sponsors [Internet]. [a.yer 04 Mart 2026]. Erişim adresi: https://www.propharmagroup.com/thought-leadership/fda-default-drug-approval-requirements-one-pivotal-trial-regulatory-strategy-implications
- Editor AS Senior. FDA Introduces New Framework to Advance Individualized Therapies for Ultra-Rare Diseases | Applied Clinical Trials Online [Internet]. 2026 [a.yer 04 Mart 2026]. Erişim adresi: https://www.appliedclinicaltrialsonline.com/view/fda-new-framework-individualized-therapies-ultra-rare-diseases
- Guidance on the application of the revised variations framework | European Medicines Agency (EMA) [Internet]. 2024 [a.yer 04 Mart 2026]. Erişim adresi: https://www.ema.europa.eu/en/guidance-application-revised-variations-framework
- Regulatory Intelligence – 2025 Round Up — Scendea [İnternet]. [a.yer 04 Mart 2026]. Erişim adresi: https://www.scendea.com/articles/regulatory-intelligence-2025-round-up
- TİTCK Tarafından Klinik Araştırma Başvurularında Güven Uygulamaları Kılavuzu Güncellenmiştir- Duyurular [İnternet]. [a.yer 04 Mart 2026]. Erişim adresi: https://www.zumbul.av.tr/tr/duyurular/t-tck-taraf-ndan-klinik-ara-t-rma-ba-vurular-nda-guven-uygulamalar-k-lavuzu-guncellenmi-tir
- Team F. Trends in Clinical Trials in 2025: Navigating a Transformative Landscape. Florence [Internet]. [a.yer 04 Mart 2026]. Erişim adresi: https://www.florencehc.com/blog-post/trends-in-clinical-trials-in-2025-navigating-a-transformative-landscape/


